FLT3-ITD突变是急性髓系白血病(AML)中最具侵袭性的遗传变异之一,与患者预后差、复发率高密切相关。尽管FLT3抑制剂已在临床应用中取得一定成效,但耐药和复发仍是治疗中的主要挑战。细胞衰老作为一种重要的肿瘤抑制机制,在多种实体瘤和血液肿瘤中发挥关键作用,但其在FLT3-ITD AML中的具体作用机制尚不明确。
近日,中国医学科学院血液病医院(中国医学科学院血液学研究所)竺晓凡/张英驰/杨文钰团队在《Leukemia》(IF=13.4)在线发表了题为“Targeting p16INK4a-mediated cellular senescence as a therapeutic strategy for FLT3-ITD-driven acute myeloid leukemia”的研究论文。该研究首次系统揭示了FLT3-ITD突变通过STAT5A-E2F3-EZH2轴抑制p16INK4a表达,从而逃逸细胞衰老、促进白血病进展的分子机制,并提出EZH2抑制剂联合FLT3抑制剂的新型治疗策略。
该研究通过分析多个测序数据集发现,p16INK4a低表达的FLT3-ITD AML患者预后不良。进一步机制研究表明,FLT3-ITD突变通过激活STAT5A-E2F3-EZH2信号轴,下调p16INK4a表达,从而抑制细胞衰老,形成促进恶性进展的正反馈环路。研究人员利用基因敲除小鼠模型证实,p16INK4a缺失显著加速FLT3-ITD AML的发生与发展。
更重要的是,该研究提出并验证了EZH2抑制剂与FLT3抑制剂联用的治疗策略。在体外和体内实验中,联合治疗显著恢复p16INK4a表达,诱导细胞衰老和凋亡,有效抑制白血病细胞增殖,并在患者来源异种移植(PDX)模型中显著延长小鼠生存期。
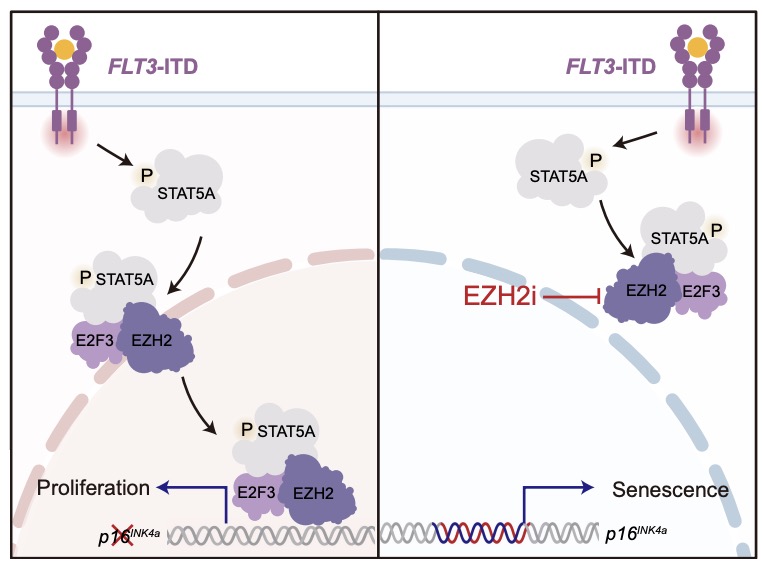
该研究不仅揭示了FLT3-ITD AML中p16INK4a调控的新机制,也为该高危亚型患者提供了新的联合治疗思路,具有重要的临床转化潜力。
中国医学科学院血液病医院(中国医学科学院血液学研究所)张英驰研究员、杨文钰主任医师和胡甜园副研究员为共同通讯作者,郑佳睿助理研究员为第一作者。该研究获科技部重点研发计划、中国医学科学院医学与健康科技创新工程、国家自然科学基金和细胞生态海河实验室创新基金等的支持。
参考文献:
1. Sun Y-M, Wang W-T, Zeng Z-C, Chen T-Q, Han C, Pan Q et al. circMYBL2, a circRNA from MYBL2, regulates FLT3 translation by recruiting PTBP1 to promote FLT3-ITD AML progression. Blood 2019; 134: 1533–1546.
2. Kottaridis PD, Gale RE, Frew ME, Harrison G, Langabeer SE, Belton AA et al. The presence of a FLT3 internal tandem duplication in patients with acute myeloid leukemia (AML) adds important prognostic information to cytogenetic risk group and response to the first cycle of chemotherapy: analysis of 854 patients from the United Kingdom Medical Research Council AML 10 and 12 trials. Blood 2001; 98: 1752–1759.
3. Oñate G, Pratcorona M, Garrido A, Artigas-Baleri A, Bataller A, Tormo M et al. Survival improvement of patients with FLT3 mutated acute myeloid leukemia: results from a prospective 9 years cohort. Blood Cancer J 2023; 13: 69.
4. Majothi S, Adams D, Loke J, Stevens SP, Wheatley K, Wilson JS. FLT3 inhibitors in acute myeloid leukaemia: assessment of clinical effectiveness, adverse events and future research-a systematic review and meta-analysis. Syst Rev 2020; 9: 285.