血友病B是编码凝血因子IX(FIX)的F9基因突变导致的一种遗传性出血性疾病,基因治疗补充正确的F9基因,修复患者的凝血系统是有望治愈该疾病的唯一方法。尽管全球范围内已有多款通过肝脏靶向腺相关病毒(AAV)递送FIX高活性突变体(FIX-Padua)基因的血友病B基因治疗产品在临床试验中取得较好疗效,但未在中国患者中系统性验证。国外已经上市的两个产品[1-2],价格昂贵,可负担性低。BBM-H901是由信念医药肖啸教授团队研发的亚洲首个血友病B基因治疗产品。早在2019年我院就开展该产品的IIT研究,2022年7月,在《The Lancet Haematology》首次发表了BBM-H901在中国血友病B患者中的IIT成果[3],展现了良好的有效性及安全性,为后继进一步系统验证药物的安全性、有效性和长期的疗效提供了坚实的依据,在IIT研究基础上,于2021年开始开展了该产品的药物注册临床研究。
2025年11月20日,中国医学科学院血液病医院(中国医学科学院血液学研究所)张磊/杨仁池团队在《Nature Medicine》(IF=50.319)在线发布了题为“Factor IX Padua gene therapy in hemophilia B: phase 1/2 and 3 trials”的药物注册研究成果。此研究证实了亚洲首个肝脏靶向血友病B基因治疗产品安全可靠,一次治疗后即可快速提升FIX:C水平,且能长期稳定保持,为血友病B患者提供了新的治疗选择与临床治愈的希望。

该研究是一项多中心、单臂、开放标签临床试验,包括1/2期及3期两部分,同时报道了1期先导试验的长期随访数据。1/2期主要目的是评估基因治疗的安全性,共入组6例受试者,均使用5×1012vg/kg。3期共入组26例受试者,按照1/2期确定的剂量给药,主要目的是评估有效性及安全性。长期随访则对1期先导试验的10名受试者(2022年发表于《The Lancet Haematology》)的FIX:C水平进行长期随访。
研究结果显示,血友病B基因治疗的安全性良好,1/2期及3期受试者均无≥3级的不良反应,无严重不良事件(SAE),无抑制物产生。最常见的与基因治疗药物相关的不良反应为肝功能异常,谷丙转氨酶(ALT)升高16.7%(1/2期)、26.9%(3期),谷草转氨酶(AST)升高33.3%(1/2期)、7.7%(3期)。通过加强免疫抑制及保肝治疗后均痊愈。
疗效方面,3期试验治疗后52周年化出血率(ABR)为0.60(95% CI: 0.18-1.99),较优效界值(中国接受预防治疗的血友病B患者平均ABR)5.0明显下降。52周时平均FIX:C为55.1(SD 35.9)IU/dL(采用SynthASil试剂的一期法)。需要特别指出的是,在基因治疗后3天时,患者平均FIX:C即达到最高值67.1(SD 23.1)IU/dL,接近后继FIX:C峰值,可以使患者迅速摆脱替代治疗。年化IX因子制品平均输注次数由治疗前的58.20(SD 30.67)下降至治疗后的2.90(SD 10.71)。关节出血次数明显下降,靶关节数目降至0。1期先导试验10名受试者长期随访结果显示,截至末次访视[中位210周(范围159-270周)],70%受试者FIX:C>35 IU/dL,其中40%可达50 IU/dL以上(采用Actin FSL APTT试剂的一期法)。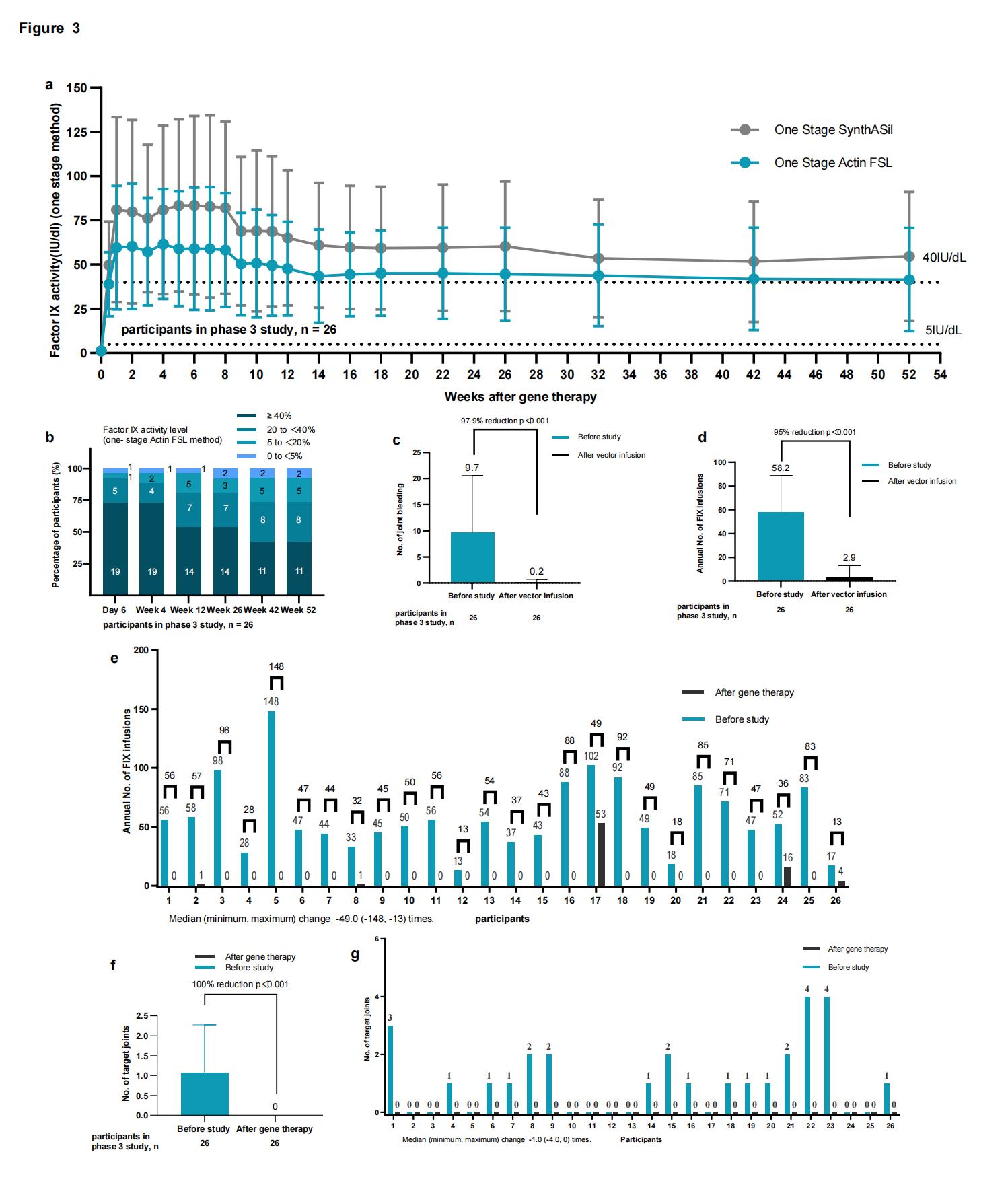
此研究通过更大的样本量,系统地证实了FIX高活性突变体(FIX-Padua)基因治疗在中国患者中安全有效。该药物不仅能快速起效,并且能维持稳定表达长达5年,使患者迅速从基因治疗中长期获益。基于3期关键试验的良好结果,国家药品监督管理局(NMPA)已于2025年4月10日批准该基因治疗产品(BBM-H901,波哌达可基注射液,商品名“信玖凝”)上市,给中国血友病B患者提供了新的治疗选择,以及治愈该病的曙光。
中国医学科学院血液病医院(中国医学科学院血液学研究所)张磊主任医师为通讯作者。中国医学科学院血液病医院(中国医学科学院血液学研究所)薛峰主任医师、鞠满凯主治医师、北京协和医院朱铁楠主任医师、昆明医科大学第二附属医院周泽平主任医师为共同第一作者。该项目获得国家重点研发计划、国家自然科学基金重点项目、中国医学科学院医学与健康科技创新工程和天津市科技项目等的支持。
参考文献:
1. Coppens, M., et al. Etranacogene dezaparvovec gene therapy for haemophilia B (HOPE-B): 24-month post-hoc efficacy and safety data from a single-arm, multicentre, phase 3 trial. Lancet Haematol 11, e265-e275 (2024).
2. George, L.A., et al. Haemophilia B Gene Therapy with a High-Specific-Activity Factor IX Variant. N Engl J Med 377, 2215-2227 (2017).
3. Xue, F., et al. Safety and activity of an engineered, liver-tropic adeno-associated virus vector expressing a hyperactive Padua factor IX administered with prophylactic glucocorticoids in patients with haemophilia B: a single-centre, single-arm, phase 1, pilot trial. Lancet Haematol 9, e504-e513 (2022).