原发性血小板增多症(ET)是一种起源于造血干细胞(HSC)的骨髓增殖性肿瘤(MPN),其特征为骨髓巨核细胞过度增生及外周血血小板持续增多。既往研究证实JAK2/CALR/MPL突变是ET的主要驱动因素[1, 2]。尽管这些突变均激活JAK-STAT通路,可导致相似的疾病表型,但不同突变携带者在疾病进展、血栓及白血病转化风险上仍存在显著异质性,这种临床表现的差异性与相似信号通路激活之间的矛盾,使得基因异质性如何影响疾病起源细胞HSC的生物学特性,成为领域内亟待阐明的核心问题。此外,缺乏已知驱动突变的三阴性(TN)ET患者,其致病机制仍是领域内长期未解的难题[3]。由于骨髓中往往共存着突变细胞与非突变细胞,传统研究手段难以从混杂群体中精准解析恶性克隆的特异性改变[4]。因此,通过单细胞基因型-转录组联合分析,系统绘制不同突变ET的HSC异质性图谱,对深入理解ET发病机制及精准干预至关重要。
2025年11月21日,中国医学科学院血液病医院(中国医学科学院血液学研究所)石莉红研究员、张磊主任医师合作在《Advanced Science》(IF=14.1)在线发布了题为“Sabotaged Integral HSC Heterogeneity Underlies Essential Thrombocythemia Development”的研究论文。研究采用单细胞转录组测序联合驱动突变检测技术,首次系统绘制不同突变亚型(JAK2、CALR、MPL及TN)ET患者HSC的单细胞转录组图谱,阐明了各亚型特异性的转录组学变化,并鉴定出跨亚型的共性致病新机制,为开发针对干细胞亚群的靶向治疗提供了新思路。

为全面解析不同突变亚型ET的致病异质性与共性致病通路,研究团队首先优化了3'-TARGET-seq单细胞测序技术,实现了对ET患者高度纯化的HSC群体进行突变基因型和转录组的同步精准检测。研究对象涵盖了JAK2、CALR、MPL突变亚型,以及TN ET患者,构建了涵盖主要亚型的、系统性的ET患者HSC异质性图谱。
研究首先解析了不同驱动突变赋予HSCs的独特分子特征。结果显示,MPL突变HSCs表现出更显著的胆固醇代谢稳态失调和内质网应激;CALR突变HSCs则高度富集细胞周期相关信号,呈现更活跃的增殖状态;分别提示了通过调节代谢通路或干预细胞周期来进行精准治疗的潜在方向。此外,在TN ET患者中,研究者锁定了一个特征性HSC亚群(C4),其同时具备高增殖与巨核偏好特征,提示转录重编程可能是驱动此类疾病的关键机制。
更为重要的是,在各亚型特异性差异的基础上,研究团队发现了一个跨越所有ET亚型的共性致病枢纽:即与趋化因子反应及淋系分化潜能密切相关的CXCR4+ HSC亚群的普遍缺失。研究发现,该亚群的缺失可直接导致HSCs的造血平衡向髓系(尤其是巨核系)分化偏移,回输该亚群可有效延缓MPN疾病进展,并显著抑制突变克隆扩增,明确了该亚群缺失在ET发病中的关键作用。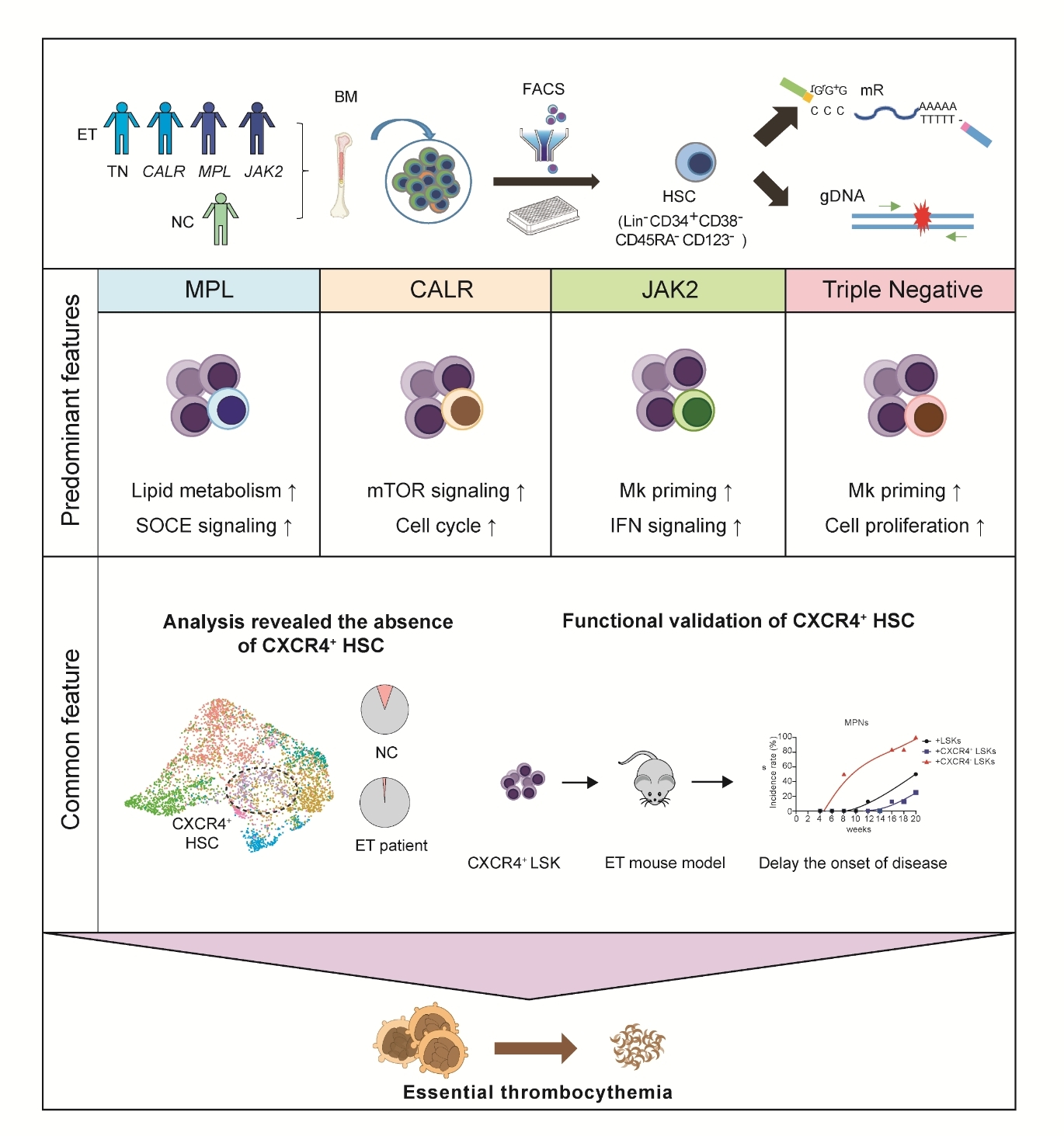
本研究不仅发现了不同驱动突变分别赋予HSCs特异性的代谢、周期和分化模式,更在TN ET中鉴定出具有致病潜能的HSC亚群。此外,研究首次阐明,HSC各亚群间存在动态互补的调控网络,其整体异质性结构的完整性对维持正常造血稳态极为重要。这些发现不仅为理解ET发病机制提供了整体性新视角,也为基于突变亚型差异的精准治疗开发提供了新的思路,更提示未来治疗策略可在传统的“清除致病细胞”基础上,融合“生态重塑”理念,通过重建HSC群体的正常组成与动态平衡,实现对MPN的多维干预。
中国医学科学院血液病医院(中国医学科学院血液学研究所)石莉红研究员、张磊主任医师为共同通讯作者,佟静媛主管技师、博士生王迪、博士生宋昊泽、孙婷主治医师、赵艳红主治医师、谷文静主治医师为共同第一作者。该项目获得国家重点研发计划、国家自然科学基金、中国医学科学院医学与健康科技创新工程以及细胞生态海河实验室创新基金等的支持。
参考文献:
1. Mead AJ, Mullally A. Myeloproliferative neoplasm stem cells. Blood. 2017;129(12):1607-16.
2. O'Sullivan J, Mead AJ. Heterogeneity in myeloproliferative neoplasms: Causes and consequences. Adv Biol Regul. 2019;71:55-68.
3. Milosevic Feenstra JD, Nivarthi H, Gisslinger H et al. Whole-exome sequencing identifies novel MPL and JAK2 mutations in triple-negative myeloproliferative neoplasms. Blood. 2016;127(3):325-32.
4. Tong J, Sun T, Ma S et al. Hematopoietic Stem Cell Heterogeneity Is Linked to the Initiation and Therapeutic Response of Myeloproliferative Neoplasms. Cell Stem Cell. 2021;28(3):502-13 e6.