靶向CD5或CD7的嵌合抗原受体T细胞(CAR-T)疗法已使众多难治性/复发性急性T淋巴细胞白血病(T-ALL)患者获得完全缓解。然而,CAR-T治疗后患者常出现严重病毒、真菌及细菌感染,较高的严重感染发生率限制了该疗法的广泛临床应用[1-4]。虽然CD5或CD7阳性淋巴细胞的显著减少是治疗后严重感染高发的重要原因之一,但残留的CD5或CD7阴性淋巴细胞是否存在功能异常、以及这些异常是否进一步加剧感染风险,目前尚不清楚。
2025年11月26日,冯晓明/潘静/姜尔烈/罗悦晨合作团队在《Advanced Science》(IF=14.1)在线发表了题为“Single-Cell Dissection Reveals Immune Dysregulation after CD5 or CD7-Directed Chimeric Antigen Receptor T-Cell Therapy”的研究论文。该研究通过单细胞测序技术,系统揭示了接受靶向CD5或CD7的CAR-T治疗后患者外周血及骨髓中免疫细胞亚群的比例和功能变化,为阐明CAR-T治疗相关免疫功能紊乱的机制以及减轻由此引发的严重感染等毒副反应提供了重要线索和新的研究方向。

该研究对来自5组共37例样本进行了单细胞RNA联合T细胞受体(TCR)/B细胞受体(BCR)测序,样本来源包括:接受CD5 CAR-T治疗患者、接受CD7 CAR-T治疗患者、接受CD19及CD22序贯CAR-T治疗患者、CAR-T治疗前T-ALL患者以及健康供者。此外,研究团队进一步通过体外功能实验,比较了在EB病毒/巨细胞病毒抗原刺激或无刺激条件下,CD5阳性T细胞、CD5天然阴性细胞及CD5敲除T细胞的功能差异,CD7阳性及CD7天然阴性T细胞的功能差异,以及CD5阳性与CD5天然阴性B细胞的表型和功能差异。
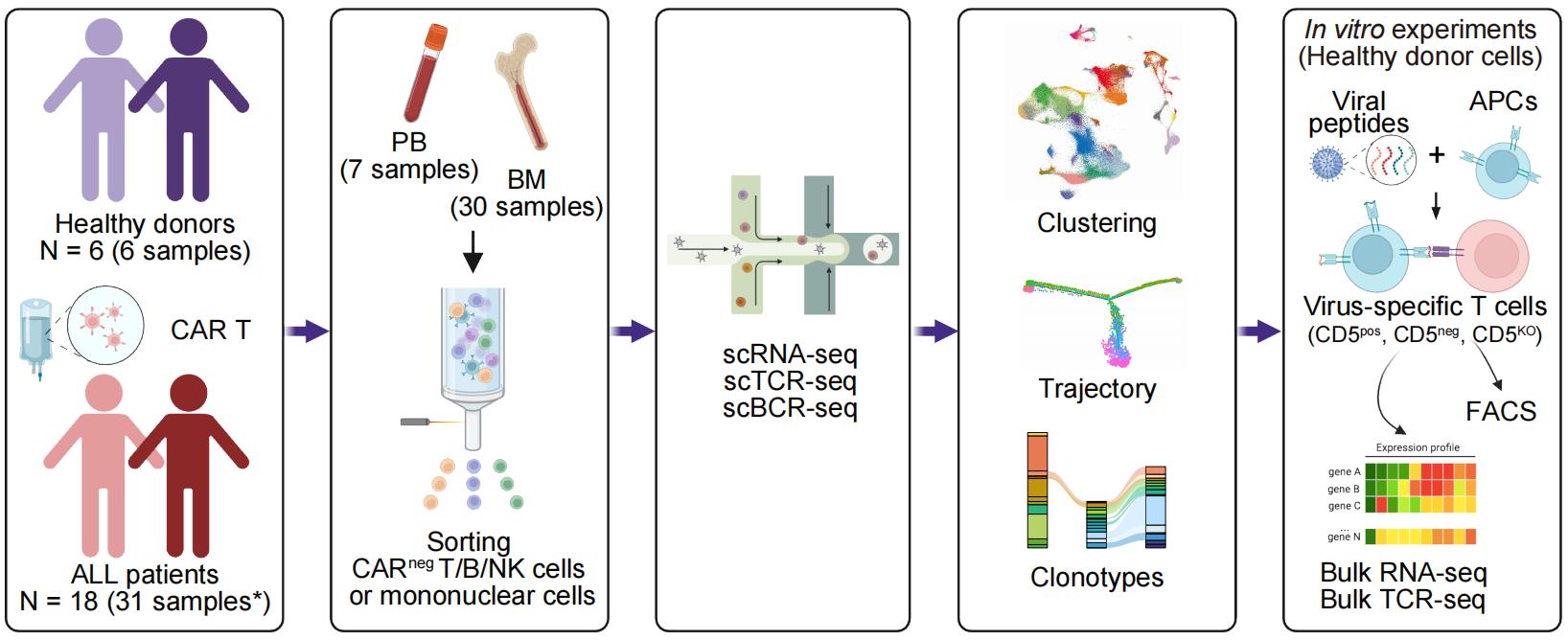
研究结果显示,CD5 CAR-T治疗后患者出现显著的T细胞耗竭,其特征为主要来源于CD5天然阴性细胞及生产过程中引入的CD5基因敲除细胞,其B淋巴细胞诱导的成熟蛋白1(Blimp-1)表达上调,同时伴随EB病毒相关性TCR克隆频率与多样性显著降低,这可能是导致严重EB病毒感染高发的重要机制之一。相较之下,CD7 CAR-T治疗引发的T细胞耗竭程度较轻,但却显著降低了针对EB病毒、巨细胞病毒、SARS-CoV-2以及细菌抗原的相关性TCR携带细胞比例,这一现象可能源于CD7天然阴性T细胞的固有功能缺陷。
B细胞、自然杀伤(NK)细胞与髓系细胞同样出现明显异常:CD5 CAR-T治疗后,B细胞表现出活化障碍、介导的适应性免疫应答减弱、BCR多样性下降、B-T细胞间相互作用受损,并伴随浆细胞异常增多;CD7 CAR-T治疗后BCR多样性亦显著降低。NK细胞在CD7 CAR-T治疗后明显减少,而CD5 CAR-T治疗对其数量无明显影响,但两种疗法均导致NK细胞呈现过度活化表型。值得注意的是,CD7 CAR-T可能通过抑制单核细胞活化并彻底清除DC细胞,削弱先天免疫功能,这可能是其高感染风险的原因之一。
尽管该研究取得重要进展,但仍存在一定局限性。由于样本量有限,目前尚未对CAR-T细胞本身及治疗前的B-ALL样本进行测序分析,也未能开展年龄分层分析及基于患者样本的体外抗原特异性T细胞功能实验,同时还需考虑体内复杂细胞相互作用的影响,后续将通过扩大样本量进一步完善相关验证。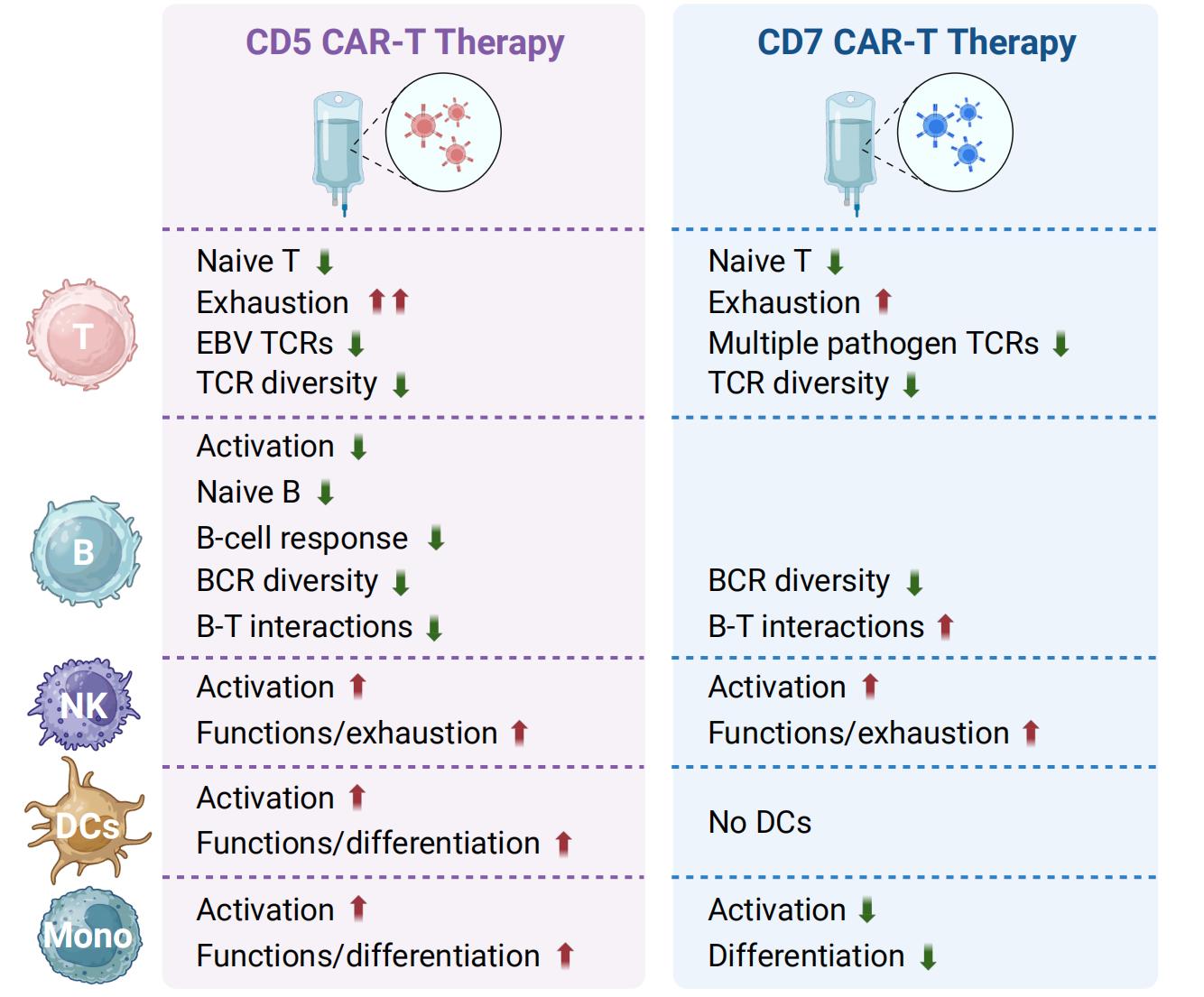
综上,与主要影响B细胞的CD19/CD22 CAR-T疗法不同,靶向CD5或CD7的CAR-T疗法可引发T细胞、B细胞、NK细胞及髓系细胞等多重免疫组分的失调。本研究首次系统揭示了上述免疫紊乱的细胞与分子特征,为T-ALL患者CAR-T治疗后严重感染的精准预防以及更安全的新一代CAR-T设计提供了理论依据与潜在干预靶点。
中国医学科学院血液病医院(中国医学科学院血液学研究所)冯晓明研究员(现工作单位为杭州师范大学)、北京高博医院潘静副主任医师、中国医学科学院血液病医院(中国医学科学院血液学研究所)姜尔烈主任医师为共同通讯作者。中国医学科学院血液病医院(中国医学科学院血液学研究所)罗悦晨副研究员、博士生张海啸、博士生唐凯婷、北京诺禾致源科技股份有限公司王一鸣博士、中国人民武装警察部队后勤学院董化江副教授为共同第一作者。该项目获得中国医学科学院医学与健康科技创新工程、国家自然科学基金、天津市科技计划项目、国家重点研发计划、国防科技创新课题等的支持。本研究工作获得中国医学科学院生物医学高性能计算平台的支持。
参考文献:
1. J. Pan, Y. Tan, L. Shan et al., Allogeneic CD5-specific CAR-T therapy for relapsed/refractory T-ALL: a phase 1 trial. Nat Med 31, 126-136 (2024).
2. J. Pan, Y. Tan, G. Wang et al., Donor-Derived CD7 Chimeric Antigen Receptor T Cells for T-Cell Acute Lymphoblastic Leukemia: First-in-Human, Phase I Trial. J Clin Oncol 39, 3340-3351 (2021).
3. Y. Tan, L. Shan, L. Zhao et al., Long-term follow-up of donor-derived CD7 CAR T-cell therapy in patients with T-cell acute lymphoblastic leukemia. J Hematol Oncol 16, 34 (2023).
4. Y. Hu, Y. Zhou, M. Zhang et al., Genetically modified CD7-targeting allogeneic CAR-T cell therapy with enhanced efficacy for relapsed/refractory CD7-positive hematological malignancies: a phase I clinical study. Cell Res 32, 995-1007 (2022).