多发性骨髓瘤(MM)是一类由恶性浆细胞克隆性增殖引起的血液系统肿瘤,其发生、进展不仅依赖基因损伤,还受到肿瘤微环境(TME)深刻影响[1]。大量研究表明,TME中的多种免疫细胞亚群,包括调节性T细胞、调节性B细胞、髓系抑制性细胞及基质细胞均可促进骨髓瘤细胞生长[2]。然而,关于固有免疫尤其是单核细胞在MM中的数量变化、功能重塑及其对免疫抑制形成的贡献,仍缺乏系统性的单细胞解析。本研究基于大规模外周血/骨髓单细胞图谱,旨在解析MM单核细胞的特征及其功能性重编程机制。
2025年11月30日,中国医学科学院血液病医院(中国医学科学院血液学研究所)安刚主任医师、邱录贵主任医师团队在《Advanced Science》(IF=14.1)在线发表题为“Type I Interferon Pathway Activation Disrupts Monocyte Maturation and Enhances Immune Evasion in Multiple Myeloma”的研究论文。本研究构建了MM患者外周血与骨髓单核细胞的单细胞图谱,发现其呈现显著增强的I型干扰素反应,揭示该信号驱动的异常发育路径在免疫抑制形成中的关键作用。

本研究从健康对照与新诊断MM患者外周血与骨髓中分选单核细胞,获得了超过13万个高质量单细胞转录组。研究共识别7类骨髓及外周血单核细胞亚群,包括经典、过渡及非经典单核细胞,并揭示了不同组织来源的显著转录差异。差异分析显示,与HD相比,MM单核细胞整体异质性变化有限,但呈现泛亚群增强的I型干扰素反应。通过发育轨迹重建进一步发现MM患者单核细胞呈现一条异常的由IFN驱动的发育路径,不同于传统由经典向非经典单核细胞分化的生理性发育路径。
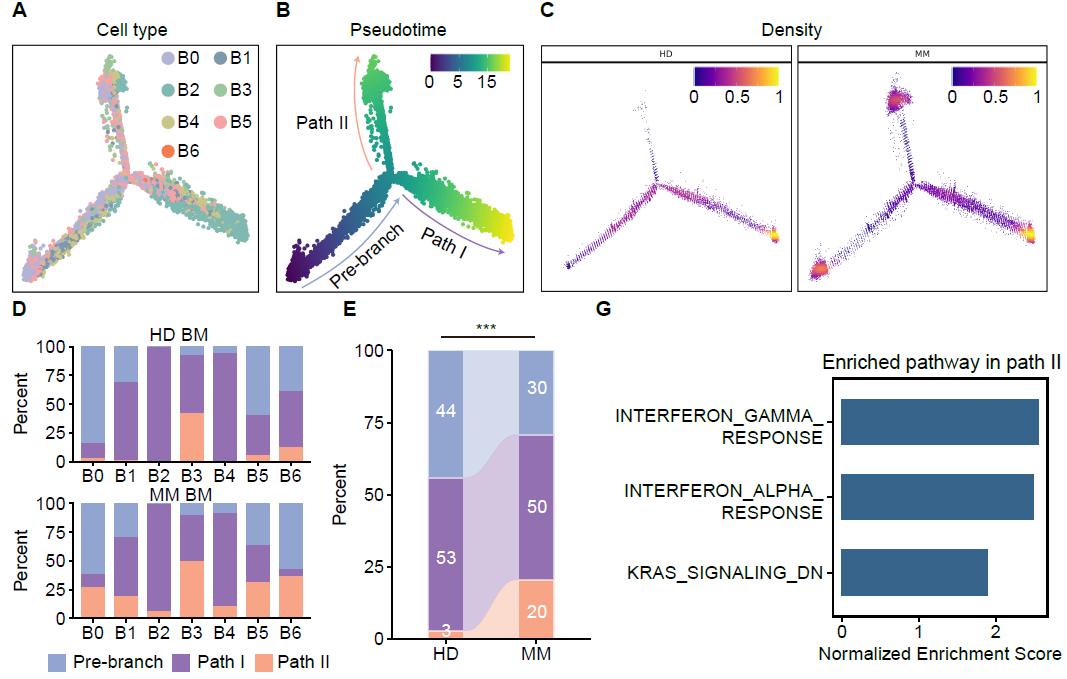
体外共培养实验显示,单核细胞与MM细胞互相诱导IFN信号激活,单核细胞分泌的干扰素α促进MM细胞增殖,且该效应可被IFNAR1中和抗体阻断。在独立随访队列中,诱导治疗显著降低MM患者骨髓单核细胞的IFN高反应状态,并增强炎症因子表达,提示抗瘤治疗可在微环境层面逆转单核细胞的慢性激活。
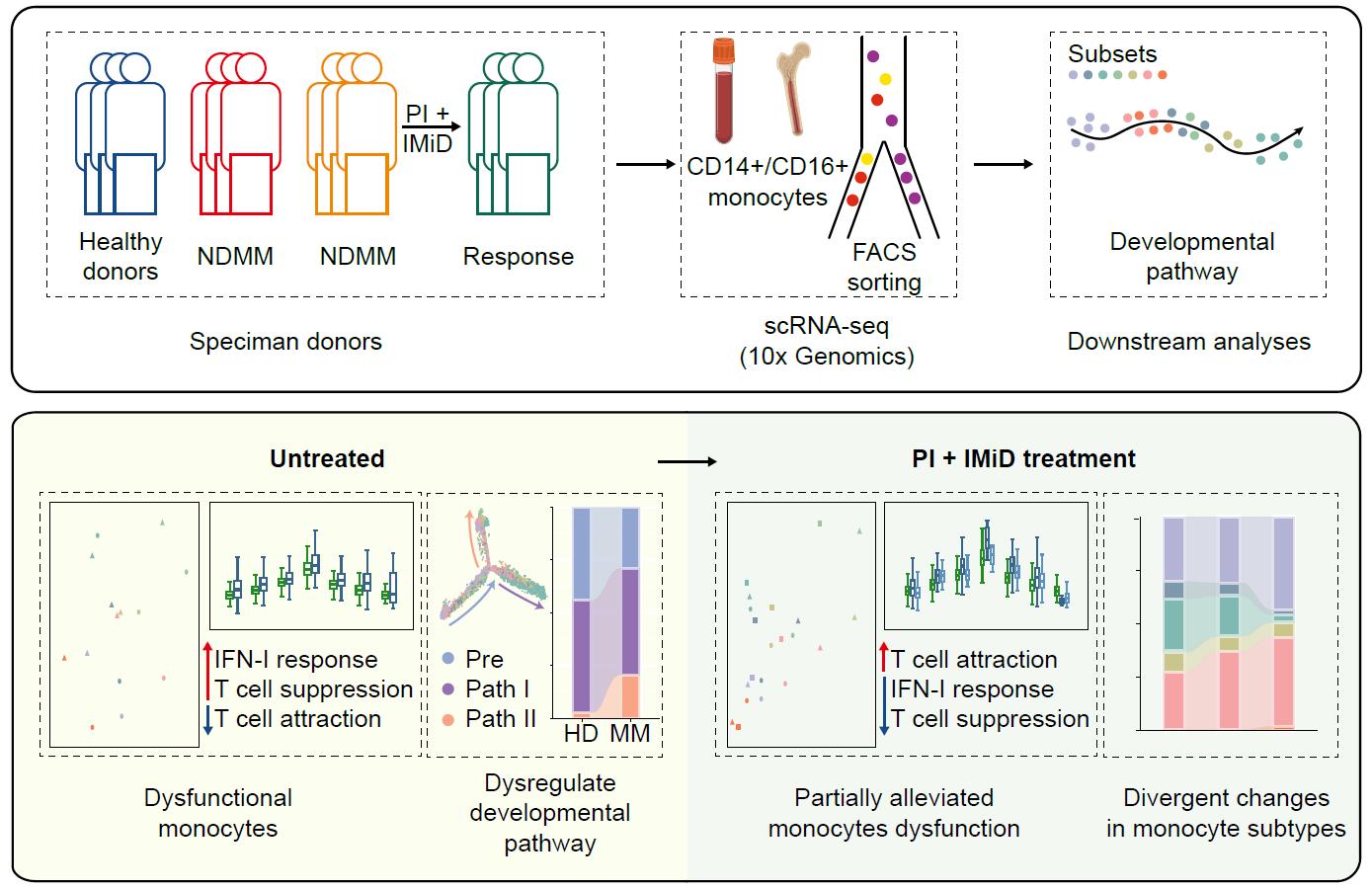
本研究发现MM患者单核细胞普遍存在过度的I型干扰素反应,揭示了该信号驱动的异常分化路径在免疫抑制性TME形成中的核心作用。研究为开发靶向I型干扰素信号轴的MM治疗策略提供了理论基础,对优化MM免疫治疗具有重要意义。
中国医学科学院血液病医院(中国医学科学院血液学研究所)安刚主任医师、邱录贵主任医师为共同通讯作者,博士生崔健为第一作者。该项目获得国家自然科学基金、科技创新2030重大专项、中国医学科学院医学与健康科技创新工程等基金的支持。
参考文献:
1. Kumar SK, Rajkumar V, Kyle RA, et al. Multiple myeloma. Nat Rev Dis Primers. 2017. 3: 17046.
2. An G, Acharya C, Feng X, et al. Osteoclasts promote immune suppressive microenvironment in multiple myeloma: therapeutic implication. Blood. 2016. 128(12): 1590-1603.