原发性骨髓纤维化(PMF)表现为骨髓网状纤维与胶原纤维的沉积、炎症细胞因子显著升高、贫血以及髓外造血,是MPN中预后最差的亚型[1]。尽管JAK抑制剂芦可替尼能缩小骨髓纤维化(MF)患者的脾脏体积并缓解体质性症状,但仍无法逆转骨髓纤维化[2]。单核细胞是MF患者炎症因子的重要来源并分化为纤维细胞来促进骨髓纤维化进展[3]。然而,单核细胞与骨髓纤维化的具体分子机制仍不清楚,需进一步深入解析其关键分子调控通路。
2025年12月17日,中国医学科学院血液病医院(中国医学科学院血液学研究所)肖志坚/李冰团队在《Blood》(IF=23.1)在线发表题为“The role of CD38 in monocytes during fibrotic progression of myeloproliferative neoplasms”的研究论文。首次发现靶向抑制CD38恢复烟酰胺腺嘌呤二核苷酸(NAD+)水平能够有效延缓骨髓纤维化的进展,高表达CD38的单核细胞能够作为预测骨髓纤维化进展的重要标志物。

研究团队构建了Mx1-Cre控制下的NrasG12D/+合并Jak2V617F/+双突变小鼠模型,双突变小鼠骨髓单核细胞水平明显升高并发生MF,体外单核细胞来源的纤维细胞数目明显增多,增多的纤维细胞主要来源于Ly6chigh单核细胞亚群。
对Ly6chigh单核细胞进行转录组测序发现MF小鼠单核细胞CD38表达显著升高,CD38作为NAD+水解酶,催化NAD+分解为烟酰胺(NAM)和ADP-核糖(ADPR)。类靶向代谢组学证实纤维化小鼠单核细胞中NAD+及其前体烟酰胺单核苷酸(NMN)水平显著降低,催化NAD+后的产物NAM及ADPR显著升高。对患者样本进行分析发现,与健康对照、慢性粒单核细胞白血病(CMML)或原发性血细胞增多症(ET)相比,MF患者单核细胞中CD38的表达水平显著升高,伴1级骨髓纤维化的真性红细胞增多症(PV)患者CD38表达水平显著高于无纤维化患者。回顾性分析发现进展为MF的PV和ET患者基线单核细胞的CD38表达水平显著高于未进展MF的PV和ET患者。
机制研究发现骨髓微环境中的炎症因子TNFα能够显著刺激CD38表达升高并伴随NAD+水平降低,进而影响Sirt1活性,导致P65蛋白的乙酰化水平升高,激活NF-κB信号通路,导致炎症微环境的扩大,促进骨髓纤维化的进展。应用CD38酶活性抑制剂78c和补充NMN能够恢复NAD+水平并抑制MF患者和小鼠单核细胞向纤维细胞的分化,体内应用78c能够有效延缓小鼠骨髓纤维化进展,为临床上缓解骨髓纤维化提供了一种新型且具有潜力的治疗策略。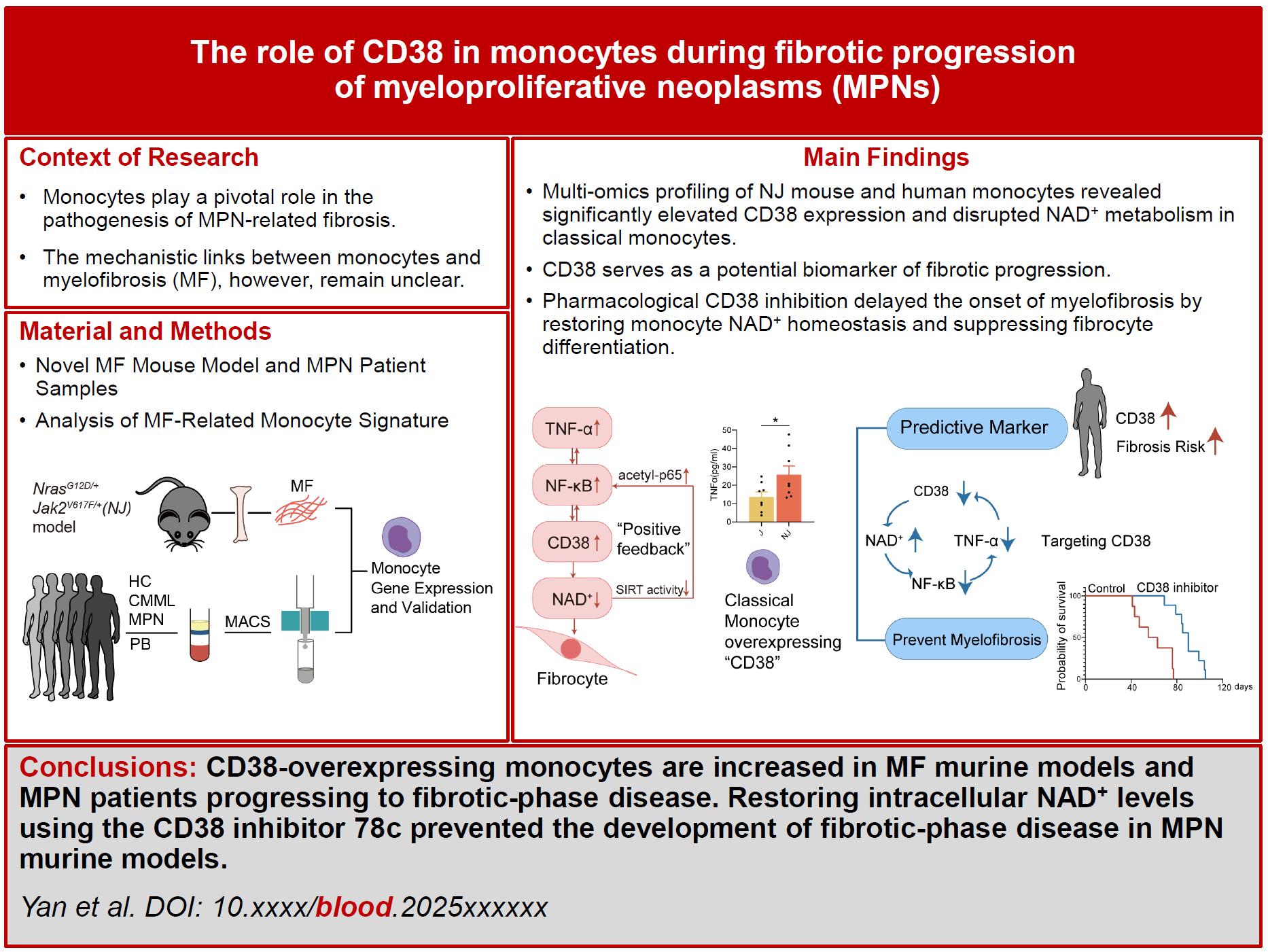
综上所述,该研究系统揭示了高表达CD38单核细胞在MF发生与进展中的重要作用,CD38抑制剂78c通过恢复细胞内NAD+水平有效延缓MF的进展,高表达CD38的单核细胞能够作为一种新型生物标志物有望预测PV和ET患者的MF进展。
中国医学科学院血液病医院(中国医学科学院血液学研究所)李冰副主任医师和肖志坚教授为共同通讯作者,闫怡汝博士和刘晋琴主管技师为共同第一作者。该项目获得国家自然科学基金、中国医学科学院医学与健康科技创新工程、细胞生态海河实验室创新基金、天津市科技计划项目等的支持。
参考文献:
1. TEFFERI A. Primary myelofibrosis: 2023 update on diagnosis, risk-stratification, and management[J]. Am J Hematol, 2023, 98(5):801-821.
2. HARRISON C, KILADJIAN J J, AL-ALI H K, et al. JAK inhibition with ruxolitinib versus best available therapy for myelofibrosis[J]. N Engl J Med, 2012, 366(9):787-98.
3. VERSTOVSEK S, MANSHOURI T, PILLING D, et al. Role of neoplastic monocyte-derived fibrocytes in primary myelofibrosis[J]. J Exp Med, 2016, 213(9):1723-40.