铁过载为铁元素在体内过度积累,导致一系列组织脏器结构损伤和功能障碍的综合征,常见于再生障碍性贫血、骨髓增生异常综合征等长期依赖输血治疗的难治性贫血疾病。目前临床上可用的铁螯合剂有限且存在副作用及依从性差等问题,导致伴铁过载的难治性贫血患者难以坚持祛铁治疗。机体长期处于高铁负荷状态会持续损伤肝脏、心脏、内分泌腺等组织器官,并损害造血与免疫系统,不利于原发病的治疗与长期预后。因此,开发副作用更小且又具有促造血作用的新型铁螯合剂,具有重要的临床应用价值[1-5]。
近日,中国医学科学院血液病医院(中国医学科学院血液学研究所)张凤奎/赵馨团队在《HemaSphere》(IF=14.6)在线发表了题为“Longitudinal clinical and preclinical studies identify hetrombopag as a potent chelator for systemic iron overload”的研究论文。该研究通过纵向临床队列与临床前研究鉴定血小板生成素受体激动剂(TPO-RA)海曲泊帕(HPAG)为强效的铁螯合剂,可预防与治疗系统性铁过载。

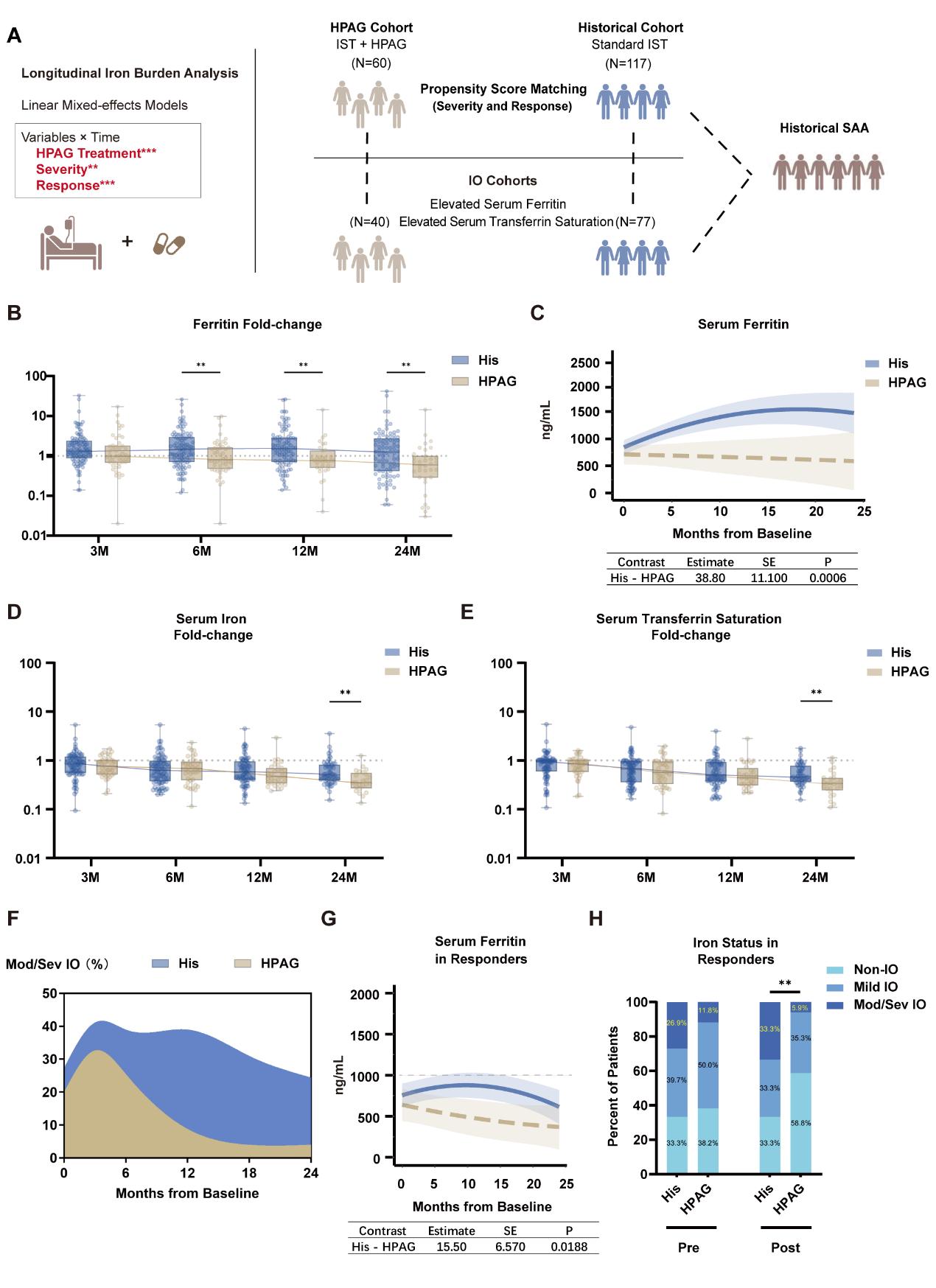
该研究首先对接受标准免疫抑制治疗(IST)的重型再生障碍性贫血(SAA)患者铁负荷进行了系统的纵向分析,发现相当一部分患者在确诊时及随访过程中已出现输血相关铁过载,并伴随体内毒性铁及脂质过氧化物的积累。在模拟输血相关铁过载的临床前模型中,研究发现HPAG能够有效治疗系统性铁过载,其铁螯合作用与临床可用的铁螯合剂相当,并在机制上独立于TPO-RA作用。随后,通过线性混合效应模型和倾向得分匹配方法,在接受IST联合HPAG治疗的临床队列中证实,HPAG能够显著降低SAA患者的铁负荷,并减少体内毒性铁及脂质过氧化物的积累。在既往已存在铁过载或具有铁过载风险的患者中,HPAG能够有效预防和治疗继发性铁过载,其带来的获益超出了TPO-RA作用本身。
该研究首次系统阐明HPAG为一种强效铁螯合剂,同时具有铁死亡抑制作用,可有效减少毒性铁的积累,抑制铁依赖性的脂质过氧化,并缓解铁过载导致的系统性损伤。上述发现为铁过载相关疾病的治疗提供了新的思路,对优化再生障碍性贫血等疾病的综合治疗策略具有重要意义。
中国医学科学院血液病医院(中国医学科学院血液学研究所)赵馨主任医师、张凤奎主任医师和中国医学科学院肿瘤医院李斯丹主任医师为共同通讯作者。中国医学科学院血液病医院(中国医学科学院血液学研究所)赵雨霏博士与博士生邢凌霄为共同第一作者。该研究获得国家重点研发计划、国家自然科学基金以及中国医学科学院医学与健康科技创新工程等项目的支持。
参考文献:
1. Brittenham, G.M., Iron-chelating therapy for transfusional iron overload. N Engl J Med, 2011. 364(2): p. 146–156.
2. Adams, P.C., G. Jeffrey, and J. Ryan, Haemochromatosis. Lancet, 2023. 401(10390): p. 1811–1821.
3. Olynyk, J.K. and G.A. Ramm, Hemochromatosis. N Engl J Med, 2022. 387(23): p. 2159–2170.
4. Coates, T.D., Management of iron overload: lessons from transfusion-dependent hemoglobinopathies. Blood, 2025. 145(4): p. 359–371.
5. Leitch, H.A. and R. Buckstein, How I treat iron overload in adult MDS. Blood, 2025. 145(4): p. 383–396.