血友病A是一种由编码凝血因子VIII(FVIII)的基因(F8)突变导致的遗传性出血性疾病,占血友病总人群的85%。重型血友病A患者自出生起即会反复出现关节等部位的自发性出血,若未能规范接受外源性FVIII蛋白替代治疗,多数患者最终将进展为关节残疾,严重影响正常学习与生活质量,因此需终身依赖外源性FVIII治疗,对社会和家庭构成沉重负担。基因治疗是治愈该疾病的唯一手段。目前,国际上仅有一款腺相关病毒(AAV)载体介导的血友病A基因治疗产品获批上市[1],价格高昂,可及性有限,且研究显示治疗后载体来源的FVIII表达水平随时间呈逐年下降趋势[2-4]。
2026年3月11日,中国医学科学院血液病医院(中国医学科学院血液学研究所)张磊/杨仁池团队在《Signal Transduction and Targeted Therapy》(IF=52.7)在线发布了题为“Phase 1 pilot study for hemophilia-A: AAV8 vector with prophylactic tacrolimus-glucocorticoid achieves therapeutic FVIII activity”的研究论文。该研究报道了在中国血友病A重型患者采用AAV基因治疗后的疗效,试验结果表明我国自主研发的首个肝脏靶向型血友病A基因治疗产品GS001(现称GS1191-0445)具有良好安全性及疗效,两个剂量组患者输注AAV产品后,FVIII水平在七天内迅速升至高水平,显示出GS001在基因递送和表达效率方面的优势。在低剂量组,GS001仍能实现高效的FVIII表达,两年期表现与国际同类疗法相当,甚至部分指标超越国际同类疗法。低剂量治疗策略还能降低治疗成本,提高血友病A基因治疗药物的可及性和可负担性,对发展中国家患者更友好。
针对AAV基因治疗血友病A后长期疗效下降这一国际挑战,该研究开创了预防性使用糖皮质激素联合他克莫司的免疫抑制方案,在不影响患者抗感染能力的前提下,有效降低了治疗过程中的免疫反应,确保目的蛋白(FVIII)的表达与活性(FVIII:C)的长期维持,提供了重要临床策略参考。

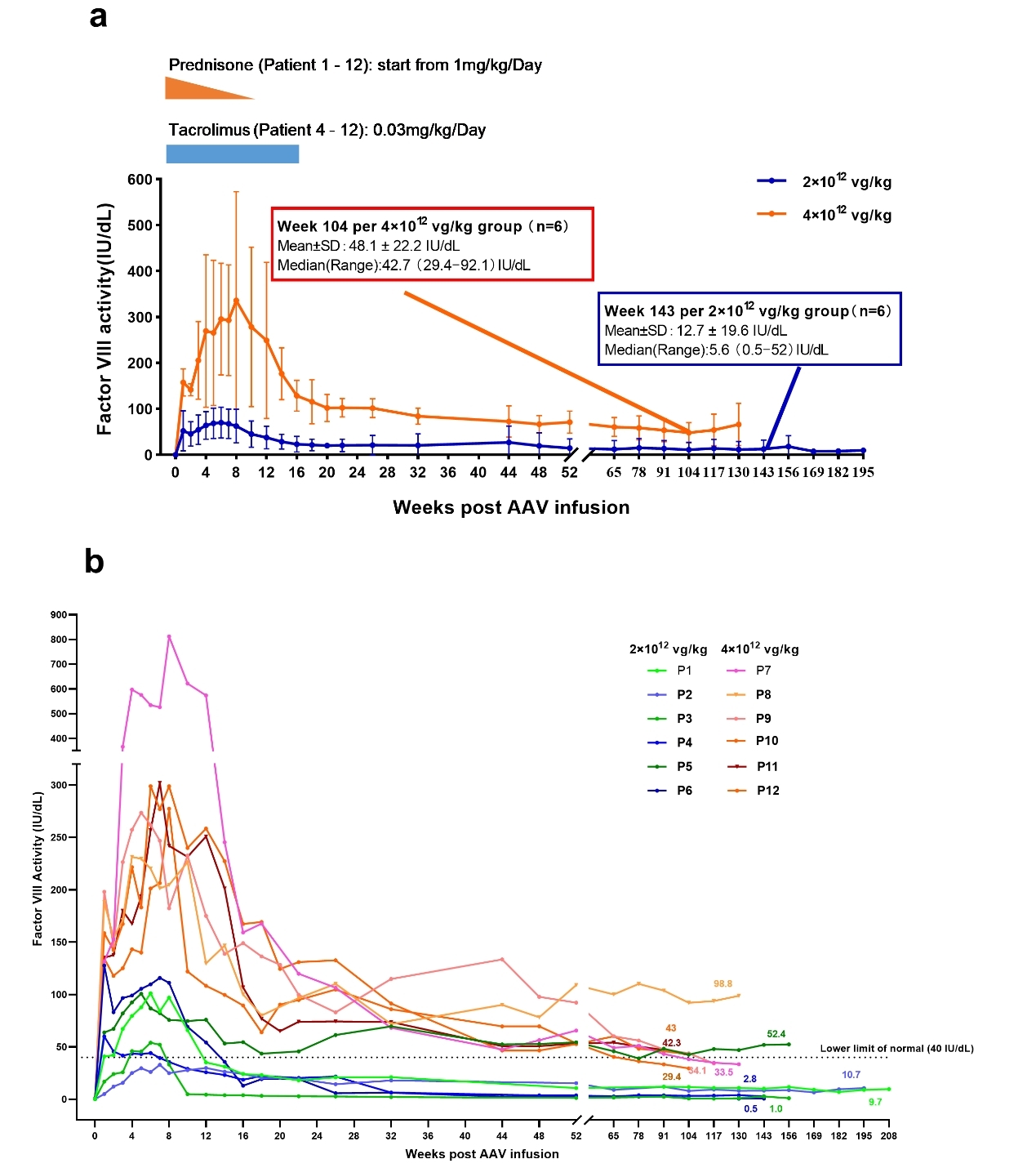
该研究是一项单中心、单臂、开放标签临床试验,共有2个剂量组:低剂量组(2×1012vg/kg)与高剂量组(4×1012vg/kg),每组6例患者,主要目的是评估有效性及安全性。
研究结果表明AAV基因治疗血友病A的安全性良好,所有受试者均无≥3级的不良反应,无严重不良事件(SAE),无抑制物产生,无血栓与栓塞事件发生。在低剂量组中,最常见的治疗期不良事件(TEAEs)是丙氨酸氨基转移酶(ALT)和乳酸脱氢酶(LDH)升高,各有3/6例(50%)。在高剂量组中,最常见的TEAEs为FVIII:C升高(>150.0 IU/dL),共6/6例(100%),常见于GS001治疗后三周内;其次为ALT和AST升高,有5/6例(83.3%)。经过治疗,两组患者转氨酶均恢复至正常水平。
在低剂量组疗效方面,患者输注GS001后,外周血FVIII:C中位数在一周内迅速升至50.4 IU/dL(范围:5.0-127.7 IU/dL),并于5.5周(范围:1.0-7.0周)达到峰值80.4 IU/dL(范围:32.9-127.7 IU/dL)。第52.0周时,FVIII:C中位水平为7.2(范围:1.3-54.3)IU/dL。第144.0周时,FVIII:C中位水平为5.6(范围:0.5-52.0)IU/dL。
在高剂量组疗效方面,患者输注GS001后,外周血FVIII:C中位数在一周内迅速达到146.9(范围:131.6-198.1)IU/dL,随后进一步升高,并于6.5周(范围:4.0-8.0周)达到峰值288.2(234.1-812.3)IU/dL。第52.0周时为59.6(范围:52.7-109.0)IU/dL。第104.0周时,FVIII:C中位数为42.7(范围:29.4-92.1)IU/dL,处于非血友病状态(>40.0 IU/dL)。
在AAV治疗后免疫反应机制方面,CD8⁺ T细胞在机体对AAV载体的免疫反应中起关键促进作用,可能导致目的蛋白表达减少、疗效降低。对临床试验患者来源外周血免疫细胞单细胞RNA分析显示,泼尼松联合他克莫司预处理能有效抑制AAV基因治疗后患者CD8⁺ T细胞的免疫应答。此外,该研究还筛选出可用于监测与干预的潜在新靶点,为今后更精准地抑制AAV基因治疗相关免疫反应提供了理论依据。

张磊/杨仁池团队首次在中国血友病A人群中采取AAV基因治疗并取得成功,给中国血友病A患者提供了新的治疗选择,以及治愈该病的曙光。
中国医学科学院血液病医院(中国医学科学院血液学研究所)张磊主任医师为通讯作者。中国医学科学院血液病医院(中国医学科学院血液学研究所)刘葳副主任医师和裴晓磊副研究员、苏州华毅乐健生物科技有限公司余腾辉博士、中国医学科学院血液病医院(中国医学科学院血液学研究所)徐秉岐博士后和代新岳主治医师为共同第一作者。该研究获得国家自然科学基金重点项目、中国医学科学院医学与健康科技创新工程和天津市科技计划项目等的支持。
参考文献:
1. Blair, H.A. Valoctocogene Roxaparvovec: First Approval. Drugs 82, 1505-1510 (2022).
2. George, L.A., et al. Multiyear Factor VIII Expression after AAV Gene Transfer for Hemophilia A. N Engl J Med 385, 1961-1973 (2021).
3. Leavitt, A.D., et al. Giroctocogene fitelparvovec gene therapy for severe hemophilia A: 104-week analysis of the phase 1/2 Alta study. Blood 143, 796-806 (2024).
4. Mahlangu, J., et al. Two-Year Outcomes of Valoctocogene Roxaparvovec Therapy for Hemophilia A. N Engl J Med 388, 694-705 (2023).