CRISPR激活(CRISPRa)筛选技术虽能通过激活内源基因表达进行功能获得性筛选,但受限于传统Cas蛋白体积过大,难以高效递送至原代人类细胞[1,2]。因此,开发紧凑高效的CRISPRa工具对推动原代细胞功能基因组研究和细胞治疗具有重要意义[3]。
2026年5月6日,中国医学科学院血液病医院(中国医学科学院血液学研究所)饶书权/程涛/姚瑶/程辉团队与中国科学院天津工业生物技术研究所薛超友团队合作在《Nature Communications》期刊发表了题为“Engineered dCas12f1-SAM enables robust transcriptional activation and gain-of-function screening in primary human cells”的研究论文。该研究基于结构导向工程化改造,开发了一套紧凑高效的dCas12f1-SAM转录激活系统,并在原代T细胞和造血干祖细胞(HSPCs)中实现了高效的内源基因激活及功能筛选,为细胞工程与免疫治疗提供了新的技术工具。

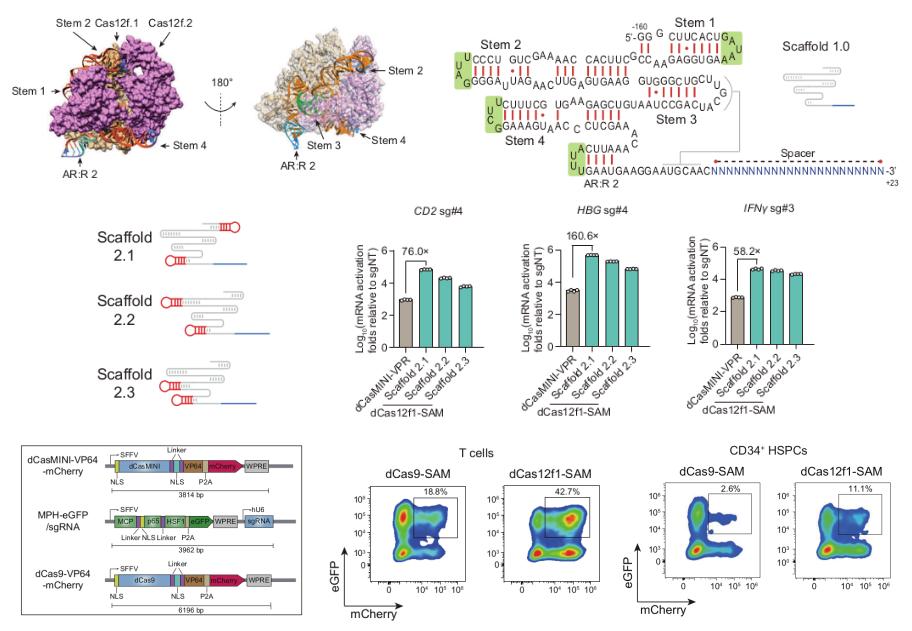
该研究设计基于协同激活介质(SAM)系统的核心原理:通过在sgRNA的支架结构部分插入MS2茎环,该结构序列可特异性识别并结合MCP蛋白,从而将MCP-p65-HSF1三元融合共激活子招募至靶基因位点,与dCasMINI-VP64协同作用,实现强效的转录激活[4]。为实现这一目的,研究团队基于Un1Cas12f1-sgRNA复合物的晶体结构,分析sgRNA支架各茎环结构在核糖核蛋白复合物(RNP)中的空间位置,将MS2适配体定点插入至游离于RNP之外的茎环位点,并经过多轮的优化设计,得到具有最强基因激活效果的scaffold 2.1结构,基于该sgRNA结构建立了dCas12f1-SAM系统。真核细胞内源性基因激活实验显示,该系统在HEK293T细胞及人原代细胞中均有较高的激活效率,较dCasMINI-VPR、dCas9-VPR、dCas9-SAM作用更为显著。全转录组RNA-seq未检测到明显的脱靶转录激活,确认该系统具有高度靶向特异性。得益于紧凑设计(dCasMINI-VP64-mCherry约3.8 kb,MPH-eGFP/sgRNA约4.0 kb),该系统在原代人T细胞和CD34+造血干祖细胞中实现了显著高于dCas9-SAM的慢病毒转导效率。这些结果确立了dCas12f1-SAM作为高效紧凑型CRISPRa工具的技术优势,明确了该系统在人原代细胞中进行基因扰动研究的可行性。
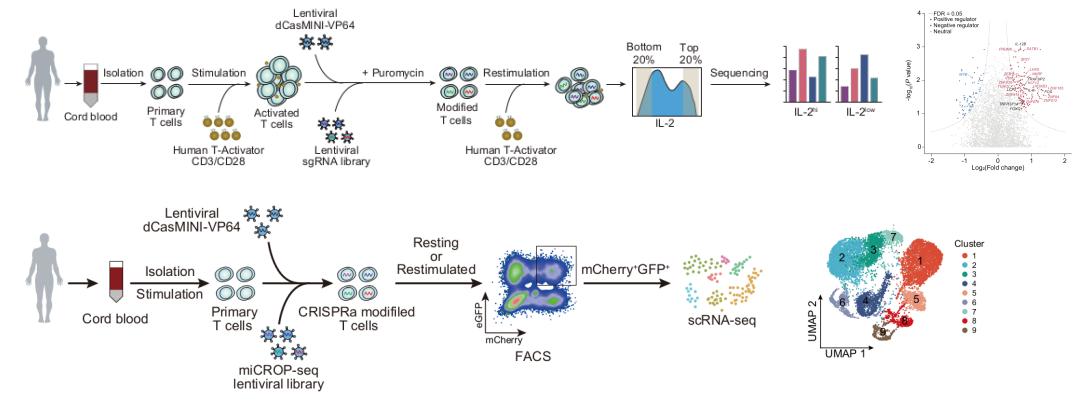
在此基础上,团队利用该系统开展了概念验证性应用研究。设计靶向1,559个人类转录因子的sgRNA文库,在原代人T细胞中进行CRISPRa筛选,最终鉴定出114个IL-2表达正调控因子和69个负调控因子。团队进一步构建了miCROP-seq单细胞分析平台,对原代人T细胞进行单细胞CRISPRa Perturb-seq分析,揭示了LHX5、KLF12等因子激活所对应的T细胞激活评分差异及独特的细胞状态聚类特征。在CD19 CAR-T细胞中过表达KLF12或LHX5,可显著增强CAR-T细胞对Raji和Nalm6肿瘤细胞抗肿瘤活性。该研究为原代细胞基因功能筛选和免疫治疗优化提供了高效的技术工具。
综上所述,该研究通过结构导向工程化改造,成功开发了一套紧凑、高效的dCas12f1-SAM转录激活系统。该系统克服了传统CRISPRa工具因体积过大而难以高效递送至原代人类细胞的技术瓶颈,实现了在原代T细胞和HSPCs中的高效基因激活和功能筛选。结合miCROP-seq单细胞分析平台,该系统可解析基因激活引发的精细细胞状态变化。KLF12和LHX5增强CAR-T细胞抗肿瘤效能的验证结果,进一步提示该系统在细胞免疫治疗和基因功能研究中的潜在应用价值。
中国医学科学院血液病医院(中国医学科学院血液学研究所)饶书权研究员、程涛教授、姚瑶研究员、程辉研究员和中国科学院天津工业生物技术研究所薛超友研究员为共同通讯作者,中国医学科学院血液病医院(中国医学科学院血液学研究所)曹佳璇博士、博士生柳志睿、陈信文硕士、博士生兰梓琳为共同第一作者。该研究获得国家重点研发计划、中国医学科学院医学与健康科技创新工程、国家自然科学基金和天津市自然科学基金等的支持。
参考文献:
1. Przybyla, L. & Gilbert, L. A. A new era in functional genomics screens. Nat Rev Genet 23, 89-103, doi:10.1038/s41576- 021-00409-w (2022).
2. Bock, C. et al. High-content CRISPR screening. Nat Rev Methods Primers 2, doi:10.1038/s43586- 022-00098-7 (2022).
3. Rao, S. et al. Dissecting ELANE neutropenia pathogenicity by human HSC gene editing. Cell Stem Cell 28, 833-845 e835, doi:10.1016/j.stem.2020.12.015 (2021).
4. Konermann, S. et al. Genome-scale transcriptional activation by an engineered CRISPR-Cas9 complex. Nature 517, 583-588, doi:10.1038/nature14136 (2015).